剖析傷口的癒合機制
瀏覽數:19740+ | 2015-08-12
撰文者 | Sophie MEYER
內容及圖片來源 | Les Nouvelles Esthétiques/全國美容雜誌社
內容及圖片來源 | Les Nouvelles Esthétiques/全國美容雜誌社
★ 外界因素(日常侵害、皮膚擦傷、灼傷、受洗滌劑刺激等)
★ 良性皮膚病(濕疹、皮炎、唇炎、脫皮性皮疹、尿布皮炎等)
★ 侵害皮膚行為(切除、縫合、脫皮、電凝固、電動脫毛、血管激光治療、激光脫毛等)
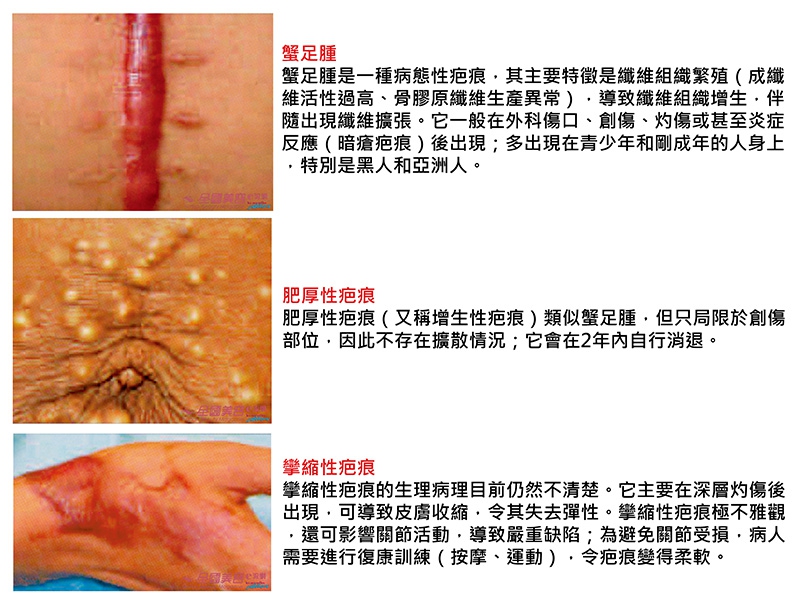
傷口癒合之目的在於重建皮膚保護層,在可能的情況下進行全面修復。癒合過程取決於眾多因素。沒有併發症的傷口癒合須要經過幾個階段,其中涉及到眾多因素。
傷口癒合的不同階段
傷口癒合是一個自然的生理過程,由機體自然啓動——在每次傷口須要修復時自然產生。這個生理過程相當複雜,涉及多種細胞(巨噬細胞、多核細胞、淋巴細胞、角朊細胞、成纖維細胞等)以及多個進程:
★ 細胞遷移
★ 細胞繁殖
★ 細胞分化
★ 細胞外間質大分子增生
傷口癒合包括由3個階段組成,重建表皮、真皮和表皮接合處,以及有大量血管的真皮。三者按具體時間順序出現,但同時亦會重疊出現:
① 血管和炎症階段
② 組織修復的繁殖階段
③ 組織重新塑形階段
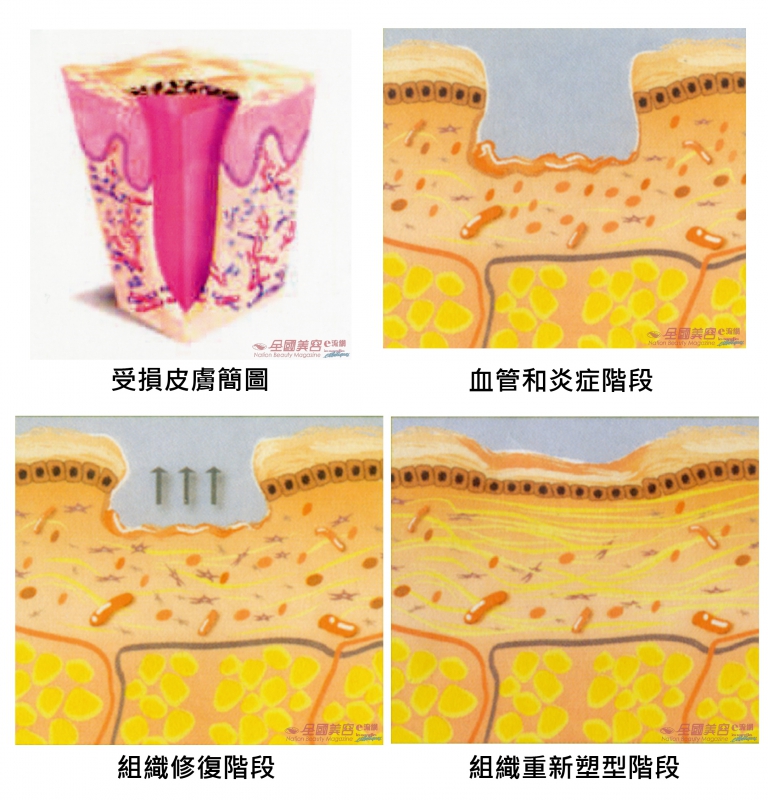
血管和炎症階段是對抗感染的階段,新細胞同時開始增生。簡單來說,這是一個「清理傷口」的階段,在傷口形成後2-4天內進行。皮膚創傷導致血管受損,從而引起血小板大量流動,血小板與骨膠原I、III接觸後會啓動血小板聚合,形成血塊,導致炎症反應的細胞開始遷移。
- 首先必須止血,血小板的職責是確保血塊形成,而血塊則支持促炎細胞遷移;其後很快便會出現滲液,從而確保有效對抗感染和清潔傷口。另外,血小板會釋放生長因子,促進傷口癒合。
- 接著,巨噬細胞、中性多核細胞介入,清除傷口中所有可能導致感染的元素。細胞因子是由參與傷口癒合的不同分子生成,從第1階段開始便刺激細胞繁殖和分裂活性。
組織修復階段
這個階段的特徵是形成全新組織和逐步填充傷口,在炎症階段(傷口出現後4天左右)後很快出現,有助形成肉芽組織(或新骨膠原),一般會持續十多天。它表現為皮膚不同的細胞組織(成纖維細胞、內皮細胞、角朊細胞)的繁殖和遷移,並按照以下2個步驟進行:
真皮修復
真皮修復有賴於:
★ 通過成纖維細胞在皮損上繁殖和遷移,形成肉芽組織,促使新骨膠原、蛋白聚糖和纖維連接蛋白的合成
★ 新血管生成,即通過內皮細胞遷移形成新的血管
★ 通過肌纖維母細胞(Myofibroblast)重建真皮和表皮接合處,因前者有助傷口兩端接合
在皮損部位的成纖維細胞之所以快速繁殖和遷移,是由於血小板和巨噬細胞生成的細胞因子與生長因子所致,它們合成細胞外間質的成分接近真皮的基本組織,後者包括:
★ 骨膠原(剛開始是III型骨膠原,其次是I型骨膠原)
★ 透明質酸、纖維連接蛋白
剛開始時,是由未成熟的真皮間質作為表皮再生的基礎;其後有賴內皮細胞遷移,則有助形成全新的血管網。
表皮修復
表皮修復乃透過位於傷口邊緣的細胞有絲分裂加快,導致以皮膚附屬器為基礎形成上皮再生,其中會產生:
★ 角朊細胞的遷移和繁殖
★ 新形成的表皮成熟與分化
★ 黑色素細胞和朗格罕氏細胞重新定殖
★ 肌纖維母細胞收縮,令傷口逐漸閉合
角朊細胞的遷移(在生長因子的刺激下形成)從傷口邊緣發展至中間部位,由傷口形成的第12小時開始,直至皮損部位被覆蓋。當傷口閉合後,角朊細胞即停止遷移,並開始繁殖;與此同時,真皮和表皮接合處由邊緣至中間部位進行合成。與角朊細胞的遷移相比,黑色素細胞和朗格罕氏細胞定殖較遲出現。
組織重新塑形階段
組織重新塑形階段是皮膚逐步恢復正常外觀的階段,可持續數月甚至數年,期間傷口癒合形成最終外觀。這階段的特徵表現是疤痕的細胞外間質成分、結構,以及細胞的性質持續逐步改變。傷口的重新塑形是根據皮膚的壓力線及以下因素進行:
★ 新血管形成減少
★ 疤痕收縮
★ 成纖維細胞轉變為肌纖維母細胞
★ 整體肉芽細胞的收縮能力
★ 出現最終骨膠原
過程
①真皮內的III型骨膠原被I型骨膠原(更具抵禦力)取代
②血管網變得更為豐厚
③透明質酸和纖維連接蛋白被骨膠原和蛋白聚糖所取代,後兩者構成的間質之牽拉力極大
④一定數量的成纖維細胞轉變為肌纖維母細胞,後者有助傷口兩端接合、收縮傷口和重塑組織
⑤角朊細胞繁殖所產生的子細胞出現細胞分化
參與傷口癒合的細胞
血小板
血小板可釋放出:
-促進血管收縮和受損血管凝固的介質;
-趨化因子和促有絲分裂因子;
-可促使傷口癒合的初始細胞過程之細胞因子。
血細胞
隨後介入的細胞包括:
-中性多核細胞:通過溶酶體酶素和吞噬作用清潔傷口;
-巨噬細胞:分泌眾多細胞因子,可刺激血管生成、增加成纖維細胞的活性和促進真皮重新塑形;
-淋巴細胞:在傷口形成後6-8天內大量出現,可促進成纖維細胞繁殖。
成纖維細胞
傷口形成48小時後,在細胞因子和生長因子釋放的作用下,成纖維細胞會在傷口內遷移和繁殖,負責合成全新細胞外間質,最初由骨膠原III構成,之後則由骨膠原I、纖維連接蛋白、蛋白聚糖(透明質酸、硫酸軟骨素等)構成。
內皮細胞
內皮細胞源自未受損的血管,在細胞因子和生長因子的作用下,有助形成全新的血管網。
角朊細胞
角朊細胞會在上皮再生時介入,並在生長因子的作用下遷移。當傷口表面覆蓋細胞層時,角朊細胞就會停止遷移,轉而開始繁殖和分化。
血小板
血小板可釋放出:
-促進血管收縮和受損血管凝固的介質;
-趨化因子和促有絲分裂因子;
-可促使傷口癒合的初始細胞過程之細胞因子。
血細胞
隨後介入的細胞包括:
-中性多核細胞:通過溶酶體酶素和吞噬作用清潔傷口;
-巨噬細胞:分泌眾多細胞因子,可刺激血管生成、增加成纖維細胞的活性和促進真皮重新塑形;
-淋巴細胞:在傷口形成後6-8天內大量出現,可促進成纖維細胞繁殖。
成纖維細胞
傷口形成48小時後,在細胞因子和生長因子釋放的作用下,成纖維細胞會在傷口內遷移和繁殖,負責合成全新細胞外間質,最初由骨膠原III構成,之後則由骨膠原I、纖維連接蛋白、蛋白聚糖(透明質酸、硫酸軟骨素等)構成。
內皮細胞
內皮細胞源自未受損的血管,在細胞因子和生長因子的作用下,有助形成全新的血管網。
角朊細胞
角朊細胞會在上皮再生時介入,並在生長因子的作用下遷移。當傷口表面覆蓋細胞層時,角朊細胞就會停止遷移,轉而開始繁殖和分化。
影響組織重新塑形所需時間的主要因素包括:年齡、基因病史、傷口位置、炎症階段的時間和程度,以及傷口的嚴重程度。
延遲傷口癒合的各種因素
傷口癒合的速度和質量首先取決於機體的整體狀態,以及傷口的狀態和位置。與此同時,傷口癒合的方式取決於以下多個因素:
感染
傷口如存在細菌及細菌過度繁殖,可導致細胞外間質逐步退化。
血液循環欠佳
靜脈功能不全可導致傷口的營養、血細胞和氧分供應不足。
凝固障礙
缺少凝固因子會影響血塊形成。
糖尿病
血糖水平的平衡對於傷口正常癒合非常關鍵,血糖過高可導致白血球出現功能性障礙,造成局部貧血的風險。
年齡增長
老年人傷口癒合的速度變慢,炎症階段進展緩慢。
營養不足
營養不良可影響炎症階段及骨膠原合成。
壓力
壓力使皮質醇增加,導致循環淋巴細胞的數量減少,令炎症反應減弱。
吸煙
吸煙會令傷口的供氧量減少,並在微細血管部位出現異常凝固的現象。
癡肥
脂肪組織的血管分布減少,令傷口壓力增加。
接受某些療程
長時間接受皮質激素療法、化療、X光治療,及服食免疫抑制藥物等。
患有某些疾病
如慢性腎功能不全、免疫力缺乏症等。
傷口癒合的障礙
傷口癒合過程有可能出現延遲或改變。最早出現的併發症就是炎症,它可阻止傷口癒合過程出現;其後還存在其他較遲出現的併發症,包括所有病態性疤痕。